ウイルス様粒子ワクチンとその下流の精製プロセス
ウイルス様粒子(VLP)ワクチンは、ウイルス構造に基づいたがウイルス遺伝物質を含んでいないワクチン技術です。彼らは、自然ウイルスの形態と表面抗原を模倣することにより、強い免疫応答を刺激し、複製できないため、より大きな安全性を提供します。 VLPワクチンは、従来のワクチンのより良い代替手段です(生きた減衰および不活性化)。 VLPワクチンは体内で複製できないため、妊娠中の女性や免疫システムの妥協を持つ女性など、すべての人に適しています。さらに、インフルエンザウイルス、アフリカの馬の病ウイルス、ブルートングウイルスなどのセグメント化されたゲノムを備えたウイルスからのカプシドタンパク質(他の構造タンパク質を含む)は、リブワクシンを減衰させるような遺伝的再併用問題のような遺伝的再結合の問題を心配することなくVLPワクチンを開発するためにも使用できます。第二に、VLPは、不活性ワクチンとは異なり、不活性化中に構造タンパク質が修飾され、免疫原性障害をもたらす可能性がある実際のウイルスの構造を模倣することができます。

イチジク。 1。VLPおよびキメラVLPの形成メカニズム
VLPワクチンの特徴
1。天然ウイルスと同様の構造:VLPは、ウイルスの1つ以上の構造タンパク質(カプシドタンパク質など)によって自己組織化され、そのサイズと形状は実際のウイルスに似ています。
2。非感染性:ウイルスゲノムは含まれておらず、疾患を複製または引き起こすことはできません。
3。高免疫原性:粒状構造は、免疫系によって効率的に認識され、B細胞およびT細胞の応答を活性化できます。中和抗体と細胞免疫を誘導することができます(例えば、HIV、HPVワクチン)。
4.安全性の高い:免疫機能が低い人(B型肝炎VLPワクチンなど)に適しています。

イチジク。 2。利用可能なVLPワクチン
VLPワクチン生産システム
VLPは、さまざまな表現システムを通じて生成できます。一般的なプラットフォームには以下が含まれます。
1。昆虫細胞 - ブキュロウイルスシステム:
利点:高収量、低コスト、複雑なタンパク質アセンブリに適しています。
アプリケーション:HPVワクチン、エボラワクチン。
2。哺乳類細胞(例:HEK293細胞):
利点:翻訳後の修正は人間に近く、包まれたVLP(インフルエンザワクチンなど)に適しています。
3。酵母システム(例:Pichia pastoris):
利点:高速、低コスト、B型肝炎ワクチンで使用されています。
4。植物システム(たとえば、タバコ葉緑体):
開発中の環境にやさしくスケーラブルな(例えば、ノロウイルスVLPワクチン)。
VLPワクチンの下流精製プロセス
VLPS発現システムの多様性は、下流の精製プロセスの不正につながります。
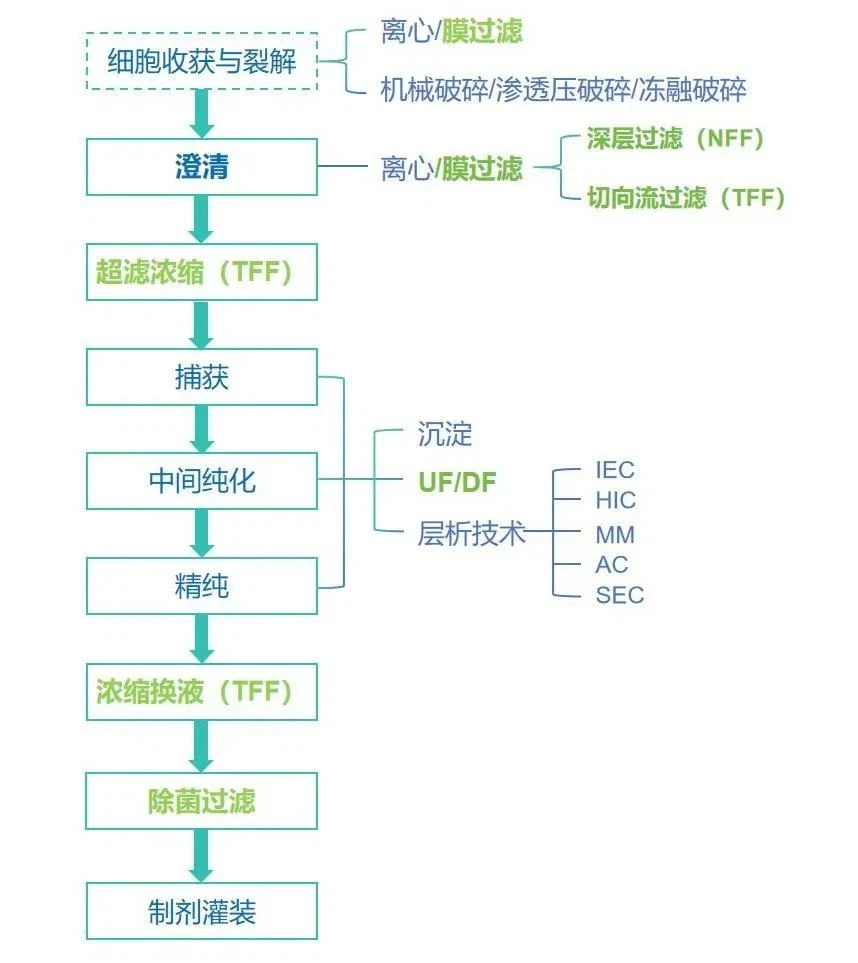
イチジク。 3一般的なダウンストリームプロセスフローチャート
収穫と明確化:
細胞培養による培地のあらゆる種類の培地では、多数のウイルス粒子、多くの細胞組織の破片、代謝生成物、およびその他の不純物があり、培地培地または半粘液を直接濃縮すると、限外ろ過膜を遮断すると、濃度は完成できず、拡張膜が濃縮されません。したがって、濃度培地内の大きな粒子を除去するために、濃度の前に最初に明確にする必要があります。そうすれば、それが半透明または透明な溶液になり、培養培地の濃度が濃度プロセスを正常にし、超促進膜のサービス寿命を確保できます。培養溶液の濃度前の明確化は、集中の過程における重要な技術的リンクです。
効率的な明確化プロセスには、固体粒子を除去するための大容量の組み合わせ、高製品の収穫量、簡単なスケールアップ、および下流のオペレーティングユニットへの保護が必要です。
方法
遠心分離:微分遠心分離は大きな粒子を除去します。
深いろ過:上清を明確にするために、多段階フィルター(例えば1.2μm→0。45μm)を使用します。
接線流ろ過(TFF):大量生産に適し、サンプルを濃縮し、不純物の小さな粒子を除去します。
ただし、栽培スケールが大きすぎる場合、遠心分離には長い時間がかかり、多数の深部フィルター膜が必要になるため、消耗品のコストが大幅に増加します。同時に、細胞培養の高密度により、ディープフィルター膜の負荷が減少し、コストの増加と過剰な製品希釈が生じます。
TFF膜成分の2種類があります:フラットカセットと中空繊維。接線流ろ過(TFF)は、膜貫通圧差によって駆動されます。膜の細孔よりも小さい物質と不純物は膜を通過しますが、より大きな粒子を持つ細胞などの不純物は閉じ込められます。微小ろ過に使用される膜の細孔サイズは{{{0}}。45/0.22μmです。中空の繊維は、高密度細胞培養培地など、高固体含有量の液体を直接処理できます。遠心分離とろ過前のステップ、より少ないステップ、単純な動作、膜を、モジュール式自動生産の要件に沿って、清掃、機器の投資と運用コストを削減することで繰り返し使用できます。
限外ろ過濃度(TFF):
ターゲット:クロマトグラフィー処理の量を減らすために、クロマトグラフィー効率を改善し、クロマトグラフィーカラムを保護します。
一般に、限外ろ過(TFF)はVLPの100倍以上を濃縮することができ、ヘテロタンパク質の除去率は99%に達することができます。その中で、中空の繊維ろ過技術には、プラグが容易ではなく、柔軟な動作、長寿命、低コスト、簡単な増幅の利点があるため、濃縮および精製VLPの中空繊維を選択することをお勧めします。
濃度と精製に限外ろ過法が使用される場合、濃度の効率と品質を直接決定する適切な膜細孔サイズを選択することが非常に重要です。一方では、標的分子を効果的に捕捉して収量を確保するために膜の開口部を選択する必要があり、一方では、ヘテロタンパク質の除去効果と処理速度を完全に考慮する必要があります。したがって、最良の原理は、ターゲット分子を閉じ込めることができる最大の細孔サイズの膜を選択し、均一な細孔サイズ分布でフィルター膜を選択してみることです。
一次精製:
1。降水方法
ポリエチレングリコール(PEG)沈殿:VLPの選択的降水には、収量と純度のバランスをとるために最適化されたPEG濃度と塩濃度が必要です。
2。クロマトグラフィー
アフィニティクロマトグラフィー:
ヘパリン親和性:表面負電荷のVLPSプロパティの使用(例:HPV VLP)。
抗体結合クロマトグラフィー:特異性が高いが高価。
イオン交換クロマトグラフィー(IEX):VLP表面電荷特性に応じて、アニオン交換(Qカラムなど)または陽イオン交換(例:SPカラム)を選択し、pHおよび塩勾配を最適化して粒子の凝集を避けます。
疎水性相互作用クロマトグラフィー(HIC):いくつかの非カプセル化VLPに適したVLPS表面疎水性に基づいています。
細かい浄化:
分子除外クロマトグラフィー(SEC、ゲルろ過):
緩衝液置換を伴う残留宿主タンパク質、核酸または凝集体の除去。高解像度ですが、最終的な改良ステップとしてよく使用されます。
マルチモードクロマトグラフィー:
たとえば、イオン交換と分子ふるい効果と組み合わせたCaptoコアシリーズ樹脂は、1つのステップでさまざまな不純物を除去できます。
ウイルスの不活性化/核酸除去(必要な場合):
ヌクレアーゼ治療:ベンゾナーゼが宿主DNA/RNAを分解するなど。
UF/DF:TFFシステムを調整して、核酸と酵素の小さな断片を除去します。
集中と準備:
接線流ろ過(TFF):
バッファー(PBSや製剤バッファーなど)を変位させながら、力価を標的とするために集中します。
滅菌ろ過:
0。22μm膜ろ過により、不妊が保証されます。
典型的なケース
以下は、典型的なVLPワクチンの下流の精製プロセスです。


ガイドリングについて
Guidling Technologyは、バイオ医薬品の下流の明確化、分離、浄化に焦点を当てた生産指向のハイテク企業です。製品は、mAb、ワクチン、診断、血液産物、血清、エンドトキシン、その他の生物学的産物のろ過プロセスで広く使用されています。 Guidling Technologyには、「カセットフィルターと接線の流れろ過装置」、「中空繊維膜」、「ウイルスフィルター」、「深部膜」、「滅菌フィルターデバイス」、「遠心膜デバイス」、およびその他の製品があり、少量の生産ろ過から生産施設への生産施設まで、多数の製品ラインがあります。 Guidling Technologyはあなたと協力することを楽しみにしています!

